网友您好, 请在下方输入框内输入要搜索的题目:
题目内容
(请给出正确答案)
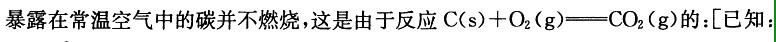
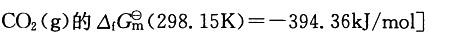

C.逆反应速率大于正反应速率 D.上述原因均不正确
参考答案
参考解析
解析:根据化学反应的摩尔吉布斯函数变化值的计算公式:


更多 “ C.逆反应速率大于正反应速率 D.上述原因均不正确” 相关考题
考题
在某温度下,反应A+B=G+F达平衡,已知ΔH﹤0,升高温度平衡逆向移动的原因是()
A.正反应速率减小,逆反应速率增大B.正反应平衡常数减小,逆反应平衡常数增大C.正、逆反应速率均减小D.正反应速率增加的倍数小于逆反应速率增加的倍数
考题
在一定条件下,使NO和O2在一密闭容器中进行反应,下列说法不正确的是()。
A.反应开始时,正反应速率最大,逆反应速率为零B.随着反应的进行,正反应速率逐渐减小,最后为零C.随着反应的进行,逆反应速率逐渐增大,最后不变D.随着反应的进行,正反应速率逐渐减小,最后不变
考题
下列叙述中,不正确的是( )。A.增加反应物的浓度可使正反应速率增加
B.反应温度升高可同时加快正、逆反应速率
C.提高反应物的浓度,可降低活化能
D.加入催化剂,可降低正、逆反应的活化能,提高反应速率
考题
下列说法正确的是( )。A.增大反应物浓度,平衡正向移动,反应物的转化率一定增大
B.正、逆反应速率改变时,平衡一定发生移动
C.对于任何可逆反应,使用催化剂只改变反应速率,不影响平衡
D.增大体系压强.化学速率加快,化学平衡一定正向移动
考题
在298K时,H2(g)+(1/2)O2(g)=H2O(L),ΔH=-285.8kJ/mol。若温度升高,则有下列中何种变化?
A.正反应速率增大,逆反应速率减小
B.正反应速率增大,逆反应速率增大
C.正反应速率减小,逆反应速率增大
D.正反应速率减小,逆反应速率减小
考题
某可逆反应的ΔrHmΘ<0,当温度升高时,下列叙述中正确的是()A、正反应速率系数增大,逆反应速率系数减小,KΘ增大B、逆反应速率系数增大,正反应速率系数减小,K减Θ小C、正反应速率系数减小,逆反应速率系数增大,K增Θ大D、正反应速率系数增大的倍数比逆反应速率系数增大的倍数小
考题
下列叙述中不正确的是()?A、增加反应物的浓度可使正反应速率增加B、反应温度升高可同时加快正、逆反应速率C、提高反应物的浓度,可降低活化能D、加入催化剂,可降低正、逆反应的活化能,提高反应速率
考题
298K时,反应N2(g)+3H2(g)→2NH3+922kJ.mol若温度升高,则()。A、正反应速率增大,逆反应速率减小B、正、逆反应速率均增大C、正反应速率减小,逆反应速率增大D、正、逆反应速率均减小
考题
对已达化学平衡的下列反应2X(g)+Y(g)2Z(g)减小压强时,对反应产生的影响是()A、逆反应速率增小,正反应速率减大,平衡向正反应方向移动B、逆反应速率增大,正反应速率减小,平衡向逆反应方向移动C、正、逆反应速率都减小,平衡向逆反应方向移动D、正、逆反应速率都增大,平衡向正反应方向移动
考题
25℃时,反应 N2(g)+ 3H2(g)=2NH3(g) ΔrHθm= -922 KJ·mol-1,若升高温度,则()A、反应速率减少,逆反应速率增大B、反应速率减少,逆反应速率也减少C、正反应速率增大,逆反应速率减少D、正反应速率增大,逆反应速率也增大
考题
在298K时,H2(g)+1/2O2(g)=H2O(L),△H=-285.8kJ/mol。若温度升高,则有下列中何种变化?()A、正反应速率增大,逆反应速率减小B、正反应速率增大,逆反应速率增大C、正反应速率减小,逆反应速率增大D、正反应速率减小,逆反应速率减小
考题
关于对行反应的描述不正确的是()。A、一切化学变化都是可逆反应,不能进行到底B、对行反应中正逆反应的级数一定相同C、对行反应无论是否达到平衡,其正逆反应的速率常数之比为定值D、对行反应达到平衡时,正逆反应速率相同
考题
单选题关于对行反应的描述不正确的是()。A
一切化学变化都是可逆反应,不能进行到底B
对行反应中正逆反应的级数一定相同C
对行反应无论是否达到平衡,其正逆反应的速率常数之比为定值D
对行反应达到平衡时,正逆反应速率相同
考题
单选题下列叙述中,不正确的是()。A
增加反应物的浓度可使正反应速率增加B
反应温度升高可同时加快正、逆反应速率C
提高反应物的浓度,可降低活化能D
加入催化剂,可降低正、逆反应的活化能,提高反应速率
热门标签
最新试卷