网友您好, 请在下方输入框内输入要搜索的题目:
题目内容
(请给出正确答案)
已知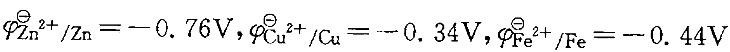 ,当在ZnSO4 (1. 0mol/L)和CuSO4(1.0mol/L)的混合溶液中放入一枚铁钉得到的产物是:
,当在ZnSO4 (1. 0mol/L)和CuSO4(1.0mol/L)的混合溶液中放入一枚铁钉得到的产物是:
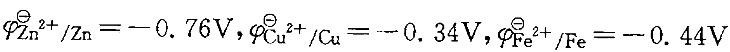 ,当在ZnSO4 (1. 0mol/L)和CuSO4(1.0mol/L)的混合溶液中放入一枚铁钉得到的产物是:
,当在ZnSO4 (1. 0mol/L)和CuSO4(1.0mol/L)的混合溶液中放入一枚铁钉得到的产物是:
A.Zn、Fe2+和Cu
B.Fe2+和Cu
C. Zn、Fe2+和H2
D.Zn和Fe2+
B.Fe2+和Cu
C. Zn、Fe2+和H2
D.Zn和Fe2+
参考答案
参考解析
解析:提示:加入铁钉是还原态,它能和电极电势比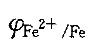 高的电对中的氧化态反应。
高的电对中的氧化态反应。
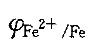 高的电对中的氧化态反应。
高的电对中的氧化态反应。
更多 “已知,当在ZnSO4 (1. 0mol/L)和CuSO4(1.0mol/L)的混合溶液中放入一枚铁钉得到的产物是: A.Zn、Fe2+和Cu B.Fe2+和Cu C. Zn、Fe2+和H2 D.Zn和Fe2+ ” 相关考题
考题
下列原电池符号正确的是。A、(-)Zn|Zn2+(1.0mol·L-1)║Cu|Cu2+(1.0mol·L-1)(+)B、(-)Zn|Zn2+(1.0mol·L-1)║Fe3+(1.0mol·L-1)|Fe2+(1.0mol·L-1)|Pt(+)C、(-)Zn|Zn2+(1.0mol·L-1)║Fe3+(1.0mol·L-1),Fe2+(1.0mol·L-1)(+)D、(-)Zn|Zn2+(1.0mol·L-1)║Fe3+(1.0mol·L-1),Fe2+(1.0mol·L-1)|Pt(+)
考题
已知原电池:(-)Zn|ZnSO4(1mol·L-1)║CuSO4(1mol·L-1)|Cu(+);若增加ZnSO4溶液的浓度,电池电动势;往CuSO4溶液中通入H2S,电池电动势。A、增加,增加B、降低,降低C、增加,降低D、降低,增加
考题
用硫代硫酸钠标定碘标准溶液,其反应式为2NaSO+I=NaSO+2NaI,已知15.0ml碘溶液,消耗了30.0ml,0.100 0mol/L的硫代硫酸钠溶液,碘溶液的浓度是A、0.050 0mol/LB、0.100 0mol/LC、0.200 0mol/LD、0.500 0mol/LE、1.000 0mol/L
考题
在1.0mol/L的,ZnSO4和1.0mol/L的CuSO4的混合溶液中放入一枚铁钉得到的产物是( )。
A.Zn、Fe2+、C.u
B.Fe2+、C.u
C.Zn、Fe2+、H2
D.Zn、Fe2+
考题
已知,当在ZnSO4 (1. 0mol/L)和CuSO4(1.0mol/L)的混合溶液中放入一枚铁钉得到的产物是:
A.Zn、Fe2+和Cu B.Fe2+和Cu
C. Zn、Fe2+和H2 D.Zn和Fe2+
考题
有一混合酸溶液,其中HF的浓度为1.0mol/L,HAc的浓度为0.10mol/L,求溶液中H+,F-,Ac-,HF和HAc的浓度已知:Ka(HF)=3.53×10-4 Ka(HAc)=1.76×10-5
考题
将铜片插入盛有0.5mol/L的CuSO4溶液的烧杯中,银片插入盛有0.5mol/L的AgNO3,溶液的烧杯中,已知:φθ(Ag+/Ag)=0.7996V, φθ(Cu2+/Cu)=0.337V写出该原电池的符号
考题
将铜片插入盛有0.5mol/L的CuSO4溶液的烧杯中,银片插入盛有0.5mol/L的AgNO3,溶液的烧杯中,已知:φθ(Ag+/Ag)=0.7996V, φθ(Cu2+/Cu)=0.337V
求该电池的电动势
考题
0.1mol/l一元弱酸HA和1.0mol/l一元弱酸HB等体积混合,混合后溶液中的氢离子浓度应为()(HAKa=1.0×10-5,HBKa=1.0×10-6)。A、2.8×10-3mol/lB、2.0×10-3mol/lC、1.0×10-3mol/lD、1.4×10-4mol/lE、1.4×10-3mol/l
考题
在30ml 1mol/L氯化钠溶液和40ml 1mol/L氯化钙溶液混合后,混合溶液中氯离子摩尔浓度为()。A、0.5mol/LB、1.0mol/LC、0.67mol/LD、2.0mol/L
考题
将铜片插入盛有0.5mol/L的CuSO4溶液的烧杯中,银片插入盛有0.5mol/L的AgNO3,溶液的烧杯中,已知:φθ(Ag+/Ag)=0.7996V, φθ(Cu2+/Cu)=0.337V写出电极反应式和原电池的电池反应
考题
在下列原电池中:(-)Zn│ZnSO4(1.0mol/L)‖C、uSO4(1.0mol/L)│C、u(+),如果降低Zn2+的浓 度,其电动势将()。A、增大B、减小C、不变D、无法判断
考题
CaCO3能溶于HAc溶液中。若沉淀达到溶解平衡时溶液中的[HAc]为1.0mol·L-1,且室温下反应产物H2CO3在水溶液中的饱和浓度为0.040mol·L-1,求1.0L溶液中能溶解()CaCO3。
考题
单选题将7.8gNaO和2.7gAl同时放入一定量的水中,充分反应后得到100mL溶液,再向该溶液中缓慢通入HCl气体3.36L(标准状况),若忽略反应过程中溶液的体积变化,则下列判断正确的是()。A
反应过程中得到3.36L(标准状况)的气体B
反应结束得到3.9g的沉淀C
反应结束得到的溶液中c(Na+)=c(Cl-)+c(OH-)D
反应结束得到的溶液中c(NaCl)=1.0mol·L-1
考题
问答题1.0mol/L的NaCl溶液500mL中含有NaCl多少克?已知NaCl的摩尔质量为58.5g/mol
热门标签
最新试卷