网友您好, 请在下方输入框内输入要搜索的题目:
题目内容
(请给出正确答案)
某元素最高氧化数为+6,最外层电子数为1,原子半径是同族元素中最小的。下列叙述中不正确的是( )。
A.外层电子排布为3d54s1
B.该元素为第四周期、ⅥB族元素铬
C.+3价离子的外层电子排布式为3d24s1
D.该元素的最高价氧化物的水合物为强酸
B.该元素为第四周期、ⅥB族元素铬
C.+3价离子的外层电子排布式为3d24s1
D.该元素的最高价氧化物的水合物为强酸
参考答案
参考解析
解析:根据题意,最高氧化数为+6的元素有VIA族和VIB族元素;而已知最外层只有一个电子,故只能是VIB族元素;在由已知中最后一个条件“原子半径是同族元素中最小的”,可确定该元素是VIB组中的Cr,Cr的电子排布式为

,可得出以下结论:
外层电子排布
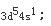
因为周期数等于电子层数,等于最高主量子数,即第四周期。他的最后一个电子填充在d亚层上,所以它是副族元素,其族数等于[(n-1)d+ns]电子层上的电子数,对Cr来讲为5+1=6,即ⅥB族元素;
因为原子失去电子时,首先失去最外层上的电子,继而再失去次外层上的d电子。所以+3价离子的外层电子排布为

Cr的最高价氧化物CrO3,其水合物为H2CrO4或H2Cr2O7均为强酸。

,可得出以下结论:
外层电子排布
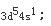
因为周期数等于电子层数,等于最高主量子数,即第四周期。他的最后一个电子填充在d亚层上,所以它是副族元素,其族数等于[(n-1)d+ns]电子层上的电子数,对Cr来讲为5+1=6,即ⅥB族元素;
因为原子失去电子时,首先失去最外层上的电子,继而再失去次外层上的d电子。所以+3价离子的外层电子排布为

Cr的最高价氧化物CrO3,其水合物为H2CrO4或H2Cr2O7均为强酸。
更多 “某元素最高氧化数为+6,最外层电子数为1,原子半径是同族元素中最小的。下列叙述中不正确的是( )。A.外层电子排布为3d54s1 B.该元素为第四周期、ⅥB族元素铬 C.+3价离子的外层电子排布式为3d24s1 D.该元素的最高价氧化物的水合物为强酸 ” 相关考题
考题
X、Y、Z、W、R是5种短周期元素,其原子序数依次增大。X是周期表中原子半径最小的元素,Y原子是外层电子数是次外层电子数的3倍,Z、W、R处于同一周期,R与Y处于同一族,Z、W原子的核外电子数之和与Y、R原子的核外电子数之和相等。下列说法正确的是A. 元素Y、Z、W具有相同电子层结构的离子,其半径依次增大B. 元素X不能与元素Y形成化合物X2Y2C. 元素Y、R分别与元素X形成的倾听合物的热稳定性:XmYXmRD. 元素W、R的最高价氧化物的水化物都是强酸
考题
下列关于B(硼)元素的叙述正确的是()A、从B的相对原子质量为10.8g,可以判断B原子核内的中子数为6B、在BCl3分子中,B原子最外层满足8电子结构C、B元素可以和H元素结合为氢化物D、硼的氢氧化物是一种强碱
考题
已知某副族元素A的原子,电子最后排入3d,最高氧化数为+4;元素B的原子,电子最后排入4p,最高氧化数为+5。回答下列问题: ⑴写出A、B元素原子的核外电子排布式。 ⑵根据核外电子排布式,指出它们在周期表中的位置(周期、族)。
考题
某元素原子主量子数n为4的电子层上有7个电子,该元素原子外层电子构型是(),未成对电子数为(),原子核外电子分布式为(),该元素原子序数是(),它位于第()周期,第()族,最高氧化数()。
考题
多选题X元素的阳离子和Y元素的阴离子具有与氩原子相同的电子层结构,下列叙述正确的是( ).AX的原子序数比Y的小BX原子的最外层电子数比Y的多CX的原子半径比Y的大DX元素的最高正价比Y的小
考题
单选题A元素原子的最外层电子数是a,次外层电子数是b;B元素原子的M层电子数是(a-b),L层电子数是(a+b)。则A、B2种元素形成的化学式可能表示为()A
B3A2B
BA2C
A3B2D
AB2
考题
单选题某元素最高氧化数为+6,最外层电子数为1,原子半径是同族元素中最小的。下列叙述中哪一个不正确()?A
外层电子排布为3d54s1B
该元素为第四周期、VIB族元素铬C
+3价离子的外层电子排布式为3d24s1D
该元素的最高价氧化物的水合物为强酸
考题
单选题X和Y均为短周期元素,X元素的阳离子和Y元素的阴离子具有相同的核外电子层结构,下列叙述正确的是( ).A
原子序数X<YB
原子半径X>YC
原子的电子层数X<YD
原子最外层电子数X>Y
考题
单选题X元素原子的最外层电子数与次外层电子数的差值等于电子层数;Y元素原子比X元素原子的最外层电子数多2。则X与Y所形成的化合物为()A
X3Y2B
X2YC
XY2D
XY3
热门标签
最新试卷