网友您好, 请在下方输入框内输入要搜索的题目:
题目内容
(请给出正确答案)
下列各电对的电极电势与H+浓度有关的是( )。
A、 Zn2+/Zn
B、 Br2/Br-
C、 AgI/Ag
D、 MnO-4/Mn2+
B、 Br2/Br-
C、 AgI/Ag
D、 MnO-4/Mn2+
参考答案
参考解析
解析:离子的浓度对电极电势有影响,四个选项的电极反应分别为:
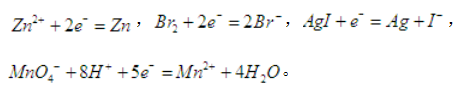
故只有D项当H+浓度变化时,电极电势才会有变化,H+浓度升高,电极电势升高。
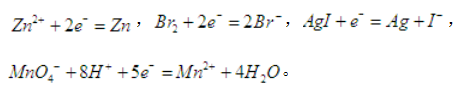
故只有D项当H+浓度变化时,电极电势才会有变化,H+浓度升高,电极电势升高。
更多 “下列各电对的电极电势与H+浓度有关的是( )。 A、 Zn2+/Zn B、 Br2/Br- C、 AgI/Ag D、 MnO-4/Mn2+” 相关考题
考题
向AgNO3、Cu(NO3)2、Zn(NO3)2的混合溶液中加入一些铁粉,反应完成后过滤,下列情况不可能存在的是()A、滤纸上有Ag、Cu、Fe、Zn,滤液中有Zn2+、Fe2+
B、滤纸上有Ag、Cu,滤液中有Zn2+、Fe2+
C、滤纸上有Ag、Cu,滤液中有Cu2+、Zn2+、Fe2+
D、滤纸上有Ag、Cu、Fe,滤液中有Cu2+、Zn2+、Fe2+
考题
在浓度均为0.10mol·L-1的Zn2+、Cd2+、Hg2+的混合溶液中,[H+]=2.0mol·L-1,向溶液中通入H2S至饱和,不生成沉淀的离子是()A、Zn2+、Cd2+B、Cd2+、Hg2+C、Zn2+D、Zn2+、Hg2+
考题
对于电池反应Cu2++Zn===Zn2++Cu,欲增加其电动势,采取的措施有下列哪种?()A、降低Zn2+浓度B、增加Zn2+浓度C、降低Cu2+浓度D、同时增加Zn2+、Cu2+浓度
考题
银锌电池 Zn│Zn2+‖Ag+│Ag 的 φθ(Zn2+/Zn) = -0.761 V, φθ(Ag+/Ag)= 0.799 V,则该电池的标准电动势 Eθ是:()A、1.180VB、2.359VC、1.560VD、0.038V
考题
对原电池(-)Zn|Zn2+(c1)‖Ag(c2)|Ag(+)而言,欲使其电动势增加可采取的措施有()。A、增大Zn2+的浓度B、增加Ag+的浓度C、加大锌电极面积D、增加Ag电极的面积
考题
溶液中pH增大时,下列电对的电极会发生哪种变化(升高、降低、不变) (1)CrO/Cr(OH):(); (2)MnO2/Mn2+:(); (3)S/H2S:(); (4)Br2/Br-:()。
考题
已知298K时,下列电极电势:φθ(Zn2+,Zn)=-0.7628V,φθ(Cd2+,Cd)=-0.4029V,φθ(I2,I-)=0.5355V, φθ(Ag+,Ag)=0.7991V, 下列电池的标准电动势最大的是:()A、Zn(s)│Zn2+‖Cd2+│Cd(s)B、Zn(s)│Zn2+‖H+│H2,PtC、Zn(s)│Zn2+‖I-│I2,PtD、Zn(s)│Zn2+‖Ag+│Ag(s)
考题
在还原性酸性溶液中,Zn的腐蚀速度较Fe为小,其原因是:()A、φ(Zn2+/Zn)(平) φ(Fe2+/Fe)(平)B、φ(Zn2+/Zn) φ(Fe2+/Fe)C、φ(H+/H2)(平,Zn) φ(H+/H2)(平,Fe)D、φ(H+/H2)(Zn) φ (H+/H2)(Fe)
考题
单选题假设规定标准氢电极的电极电势φθ(H+/H2)=1V,则测得下列原电池:(-)Zn|Zn2+(1mol·dm-3)||H+(1mol·dm-3)|H2(pθ)(Pt)(+)的标准电动势Eθ和锌标准电极电势φθ(Zn2+/Zn)的数值变化为()A
标准电动势Eθ和锌标准电极电势φθ(Zn2+/Zn)各增加1VB
标准电动势Eθ和锌标准电极电势φθ(Zn2+/Zn)各减少1VC
标准电动势Eθ不变,锌标准电极电势φθ(Zn2+/Zn)增加1VD
标准电动势Eθ不变,锌标准电极电势φθ(Zn2+/Zn)减少1VE
标准电动势Eθ和锌标准电极电势φθ(Zn2+/Zn)均不变
考题
单选题对原电池(-)Zn|Zn2+(c1)‖Ag(c2)|Ag(+)而言,欲使其电动势增加可采取的措施有()。A
增大Zn2+的浓度B
增加Ag+的浓度C
加大锌电极面积D
增加Ag电极的面积
考题
单选题对于银锌电池(一)Zn|Zn+||Ag+|Ag(+),已知(Zn2+/Zn)=-0.761V,φ(Ag+/Ag)=0.799V,该电池的标准电动势为()A
1.180VB
0.038VC
2.369VD
1.56V
热门标签
最新试卷