2021年结构工程师《基础考试(一级)》章节练习(2021-03-20)
发布时间:2021-03-20
2021年结构工程师《基础考试(一级)》考试共题,分为。小编为您整理第三章 普通化学5道练习题,附答案解析,供您备考练习。
1、已知反应当反应达平衡后,欲使反应向右进行,可采取的方法是( )。 【单选题】
A.升温,升压
B.升温,减压
C.降温,升压
D.降温,减压
正确答案:C
答案解析:此反应为气体分子数减小的反应,故升压可使反应向右进行;反应的A为放热反应,故降温可使反应向右进行。
2、下列元素电负性大小顺序中正确的是( )。【单选题】
A.Be> B> Al> Mg
B.B> Al> Be≈Mg
C.B> Be≈AI> Mg
D.B≈Al
正确答案:C
答案解析:根据电负性的变化规律,同一周期从左到右,主族元素的电负性逐渐增大;同一主族从上到下,元素的电负性逐渐减小,因此B> Be>Mg;处于对角线位置的元素Be、Al 性质相似,电负性近似相同。
3、下列分子中,属于极性分子的是( )。【单选题】
A.
B.
C.
D.
正确答案:D
答案解析:分子的正电荷中心与负电荷中心重合的分子属于非极性分子,反之,则属于极性分子。A项,02是双原子分子,结构为O-O,正负电荷中心均在双键中间,属于非极性分子; B项,CO2是直线型分子,结构为O-C-O,正负电荷中心均在碳原子上,属于非极性分子; C项,BF3 是平面三角形分子,结构为:正负电荷中心不能重合,属于极性分子。
4、 中Be的原子轨道杂化轨道类型为()。【单选题】
A.sp
B.
C.
D.不等性
正确答案:A
答案解析:sp杂化是指由一个 ns 轨道和一个p轨道组合形成两个相同的sp杂化轨道,每个sp杂化轨道含有s/2和p/2的成分,sp杂化轨道间的夹角为180°,Be 原子的电子层结构式成键时,Be 原子的一个2s电子可激发到2p轨道,使Be原子的电子层结构变为与此同时,Be原子的一个2s轨道和一个2p轨道发生杂化,形成两个sp杂化轨道,分别与两个Cl原子的3p轨道重叠,而形成两个Be-CI 键,形成的分子的空间结构呈直线形。
5、对一个化学反应来说,下列叙述正确的是( )。【单选题】
A.反应速率越快
B.反应速率越快
C.活化能越小,反应速率越快
D.活化能越大,反应速率越快
正确答案:C
答案解析:是用来判断化学反应进行方向的,对反应速率没有影响。活化能的大小与反应速率关系很大,在一定温度下,反应物的平均能量也是一-定的,而反应的活化能越大,则活化分子在全体分子中所占的比例(或摩尔分数)就越小,反应就越慢;反之,若反应的活化能越小,则活化分子的摩尔分数就越大,反应就越快。
下面小编为大家准备了 结构工程师 的相关考题,供大家学习参考。
B 杆端约束无关
C 杆横截面形状无关
D 杆的弹性模量有关
 与E有关
与E有关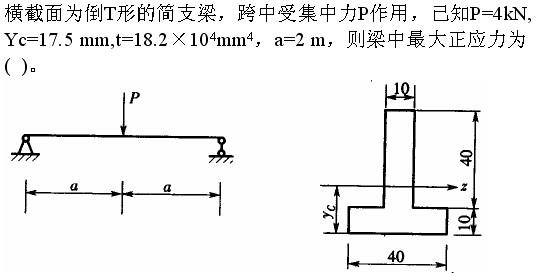
B.-385MPa
C.714MPa
D.-714MPa
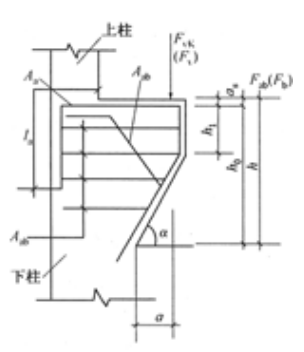
若截面的有效高度h0=810mm,则纵向受拉钢筋的截面面积As最接近于( )mm2。
B..1310
C..1400
D..1520

声明:本文内容由互联网用户自发贡献自行上传,本网站不拥有所有权,未作人工编辑处理,也不承担相关法律责任。如果您发现有涉嫌版权的内容,欢迎发送邮件至:contact@51tk.com 进行举报,并提供相关证据,工作人员会在5个工作日内联系你,一经查实,本站将立刻删除涉嫌侵权内容。
- 2020-07-25
- 2020-12-29
- 2021-07-18
- 2020-04-04
- 2020-12-18
- 2020-07-28
- 2021-07-26
- 2020-11-30
- 2020-05-17
- 2021-08-03
- 2021-02-20
- 2020-06-02
- 2021-05-05
- 2021-02-21
- 2021-01-08
- 2021-01-04
- 2021-01-05
- 2020-10-31
- 2021-04-07
- 2020-08-01
- 2020-12-28
- 2020-06-21
- 2020-09-25
- 2021-04-17
- 2020-10-11
- 2020-05-16
- 2021-04-28
- 2021-02-03
- 2021-07-26
- 2020-06-29