网友您好, 请在下方输入框内输入要搜索的题目:

即C2H2是2.5 L.所以,原混合气体中的乙烷为10L-2.5 L=7.5 L.
解此题应注意“恰好完全反应”和“都变成饱和烃”这两点.“恰好完全反应”指反应物(C2H2和H2)都无剩余,所以求得2.5 L才正确。“都变成饱和烃”说明1mol C2H2要跟2 mol H2反应.
B.38.24%
C.60%
D.40%
B.1:1
C.1:2
D.3:4
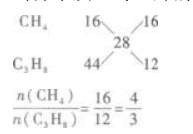
所以,甲烷与丙烷的体积比也是4:3.
(2)此题也可用其他方法计算.

升甲烷、乙烷、甲醛组成的混合气体,完全燃烧后生成15.68升(气体体积均在标准状况下测定),混合气体中乙烷的体积分数为()。
- A、0.2
- B、0.4
- C、0.6
- D、0.8
正确答案:B
在100℃和1.01×105Pa下,在乙炔和某气体X的混合物中加入足量氧气,使之充分反应,只生成CO2(g)和H2O(g)。其中CO2的体积是最初混合气体体积的1.4倍,水蒸气的体积为最初混合气体的1.6倍(体积均在同温同压下测定),则X是()。
- A、乙烯
- B、乙烷
- C、甲醇
- D、甲醛
正确答案:C
PAGE PAGE 3 有机计算型选择题解题方法归纳 1. 原子守恒法 例:1L丙烷与xL的O2混合点燃,丙烷完全反应后,生成混合气体体积为aL(气体体积均在120,测定),将aL混合气体通入足量的碱石灰后,测得剩余气体的体积为bL,若,则x的值为( ) A. 4B. 4.5C. 5.5D. 6 解析:由题意可知1L丙烷在xL的O2中燃烧生成的二氧化碳和水蒸气共为;根据H原子守恒,水蒸气的体积为4L,则为2L;所以,可知本题为不完全燃烧,又根据C原子守恒可知CO为。再根据O原子守恒得,答案为B。 2. 极值法 例:经多步裂化,最后完全转化为五种气体的混合物。该混合物的平均相对分子质量可能是( ) A. 28B. 30C. 38D. 40 解析:依题意,裂化的可能性有以下四种:,或,或,或。归纳各种产物的物质的量必须在之间,根据质量守恒定律便知平衡相对分子质量在之间,故B、C符合题意,答选B、C。 3. 通式法 例:若1mol某气态烃完全燃烧,需要,则( ) A. B. C. D. 解析:根据烃完全燃烧的通式。 依题意 当时,。 故选B。 4. 差量法 例:室温时20ml某气态烃与过量氧气混合,完全燃烧后的产物通过浓硫酸,再恢复到室温,气体体积减少了50ml,剩余气体再通过苛性钠溶液,气体又减少了40ml。则该气态烃的分子式为( ) A. B. C. D. 解析:烃完全燃烧的通式 又根据,得 故该烃的分子式为,答选B。 5. 最简式法 例:某烃的分子中碳的质量分数为80%,则它的分子式是( ) A. B. C. D. 解析:烃的分子中碳的质量分数为80%,则氢的质量分数为20%。列式为: 最简式为,分子式为。 答选B。 6. 变式法 例:下列各组物质中各有两组分,两组分各取1mol,在足量氧气中燃烧,两者消耗氧的量不相同的是( ) A. 乙烯和乙醇 B. 乙炔和乙醛 C. 乙烷和乙酸甲酯 D. 乙醇和乙酸 解析:将烃的含氧衍生物的分子式的书写形式进行变化,如乙醇,乙醛,甲酸乙酯,式中“”“”部分不消耗。 答选D。 7. 平均值法 例:常温下,将气态烷烃和烯烃按体积比5:1混合,混合气体是相同条件下等质量氢气体积的1/16,则混合气体的组成为( ) A. 甲烷和乙烯B. 乙烷和丙烯 C. 丁烷和丁烯D. 甲烷和丁烯 解析:由题意知混合气体的平均相对分子质量为32,根据平均值法否定A和C。 将B和D项代入公式计算 故选B。 亦可利用十字交叉法确定B否定D。 8. 规律法 例:两种气态烃以任意比例混合,在105时1L该混合烃与9L氧气混合。充分燃烧后恢复到原状态,所得气体体积仍为10L。下列各组混合烃中不符合此条件的是( ) A. B. C. D. 解析:显然,题给氧气对各选项物质均为过量,完全氧化产物均为CO2和水蒸气。又由于恢复到原状态,所得气体体积不变,根据烃完全燃烧的规律,可确定混合烃中的氢原子数一定等于4。再利用平均组成法确定B项不符合此条件,又由于两种气态烃必须以任意比例混合,故D项也不符合。选B、D。 9. 平均组成法 例:两种气态烃组成的混合气体,完全燃烧得和水。则混合气体中( ) A. 一定有甲烷 B. 一定是甲烷和乙烯 C. 一定没有乙烷 D. 一定有乙炔 解析:利用题中数据 根据原子守恒列式为=1:1.6:4 则得平均组成式。 因碳原子数小于2,所以混合气体中一定有甲烷。 再利用平均组成法确定另一种烃分子中的H原子数也必为4 即可能为,可能为。 选A、C。
将装有50mLNO2、NO混合气体的量筒倒立于水槽中,反应后气体体积缩小为30mL,则原混合气体中NO2和NO的体积比是()。
- A、5:3
- B、3:5
- C、2:5
- D、3:2
正确答案:D
CO、CH4、N2的混合气体20.0ml,加入一定量过量O2的燃烧后,体积缩减了21.0ml,生成CO218.0ml,计算混合气体中各组分的体积分数。
正确答案:CO 50%、CH4 40%、N2 10%。
将20gH2、O2、N2的混合气体点燃,完全反应后生成18gH2O,则剩余的气体不可能是()。
- A、H2和N2
- B、O3和N2
- C、O2和N2
- D、2gN2
正确答案:C
使1.0体积的某气态烷烃和烯烃的混合气体在足量空气中完全燃烧,生成2.0体积的二氧化碳和2.2体积的水蒸气(均在120℃、1.01×105Pa条件下测定),则混合气体中烷烃和烯烃的体积比为()
- A、2∶3
- B、1∶4
- C、4∶1
- D、3∶2
正确答案:B
2L甲醛气体与xL的氧气混合点燃,甲醛充分反应后,生成的混合气体的体积为aL(气体体积均在120°C,101kPa时测定)。将aL混合气体通过足量的碱石灰后,测得剩余气体的体积为bL。若a-b=3.5,则x的值为()。
- A、2
- B、4
- C、1.75
- D、3.5
正确答案:C
更多 “有机计算型选择题解题方法归纳” 相关考题
- 航空活塞发动机的加速性比航空燃气涡轮发动机的加速性:()A、更好B、更差C、一样D、无法比较
- 下列哪些行为是属于禁止的()A、绿地内乱设广告B、擅自砍伐树木C、借树搭棚D、树木上挂物
- 2005年版人民币取消的防伪标志是()A、隐形面额数字B、阴阳互补对印图案C、雕刻凹版印刷D、红蓝彩色纤维
- 取得会计应具备哪些条件?
- 在装备有EFIS的飞机上,通常将气象雷达系统所提供的信息显示在: ()A、EADI(电子姿态指引仪)B、EHSI(电子水平状态指示器)C、EICAS(发动机警戒及警告系统)D、CDU(控制显示主件)
- 因下列()原因确需迁移树木的,建设、养护单位或者业主应当向市或者区、县绿化管理部门提出申请。A、因城市建设需要B、已经被折损的树木C、树木对人身安全或者其他设施构成威胁D、严重影响居民采光、通风和居住安全
- 世界时是指:()A、英国伦敦的地方时B、西二区的时区时C、12时区的的时区时D、零时区的时区时
- 预定航线的磁航线角287°,航行风向150°,航线上存在什么侧风:()A、右侧风B、左侧风C、右逆侧风D、左顺侧风
- 地方性法规可以设定的行政强制措施有()。A、限制公民人身自由B、查封场所、设施或者财物C、冻结存款、汇款D、扣押财物
- 景观灯光设施的(),应当保持景观灯光设施的完好,并按照市容环境卫生管理部门规定的时间开启景观灯光设施。A、所有者B、使用者C、管理者D、租赁者